肖书奇教授团队再度揭示猪繁殖与呼吸综合征病毒继发细菌感染的新机制
猪繁殖与呼吸综合征(PRRS)俗称“蓝耳病”,是困扰全球养猪业的最重要疫病和压在我国养猪业头上的“三座大山”之一。该病导致母猪繁殖障碍和各年龄段猪只的呼吸系统疾病,造成巨大的经济损失。猪繁殖与呼吸综合征病毒(PRRSV)的一个关键致病特性是感染后会严重损害猪只的免疫系统导致免疫抑制,使猪极易感染细菌(如链球菌、副猪嗜血杆菌等),从而引发高致死率的细菌性继发感染,严重威胁养猪业的健康可持续发展。
肖书奇教授团队前期从细胞骨架重塑的角度揭示了PRRSV促进细菌入侵的继发感染新机制,2025年发表于《mBio》。
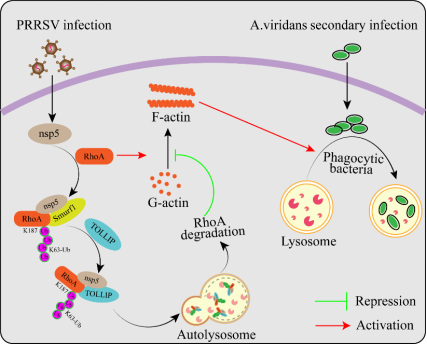
近日,该团队针对入侵的细菌如何逃逸巨噬细胞靶向清除的科学问题,以“PRRSV-2 impedes lysosomes from eliminating secondary infected bacteria”为题,在《PLOS Pathogens》发表文章。该研究发现,PRRSV感染后通过病毒非结构蛋白nsp5招募E3泛素连接酶Smurf1,诱导“肌动蛋白调节器”RhoA蛋白的多聚泛素化修饰,进一步在自噬受体TOLLIP的作用下经自噬-溶酶体途径降解RhoA蛋白。RhoA蛋白降解后,其介导肌动蛋白单体G-actin向丝状肌动蛋白F-actin的合成过程受阻,有效限制了巨噬细胞内溶酶体的定向运输,阻碍巨噬细胞靶向清除继发感染的细菌,从而利于继发感染的细菌存活。
肖书奇教授为本文通讯作者,博士研究生郑紫方、凌雪、乔双为本文共同第一作者。该研究得到国家自然科学基金、甘肃省联合基金、甘肃省重大科技专项、中国农业科学院科技创新工程等项目的资助。
该团队的两项研究从“细菌入侵”到“逃逸清除”、从“FLNA介导的骨架重塑”到“RhoA调控的溶酶体运输”、从“激活黏附入侵”到“抑制细菌清除”,较为系统性地揭示了PRRSV通过重编程细胞骨架动态平衡促进细菌继发感染的完整分子链条。这一研究体系不仅突破了传统免疫抑制机制的认知局限,建立起病毒主动重塑宿主细胞微环境的新型致病机制;更系统揭示了F-actin动态调控网络在细菌继发感染过程中的核心枢纽作用,其所鉴定的FLNA、RhoA、ITGα5等关键节点分子,也为临床干预提供了潜在的靶点群,为突破抗生素耐药困境、有效控制病毒继发感染奠定了重要的理论基础与研究思路。

